Sécurité des vaccins
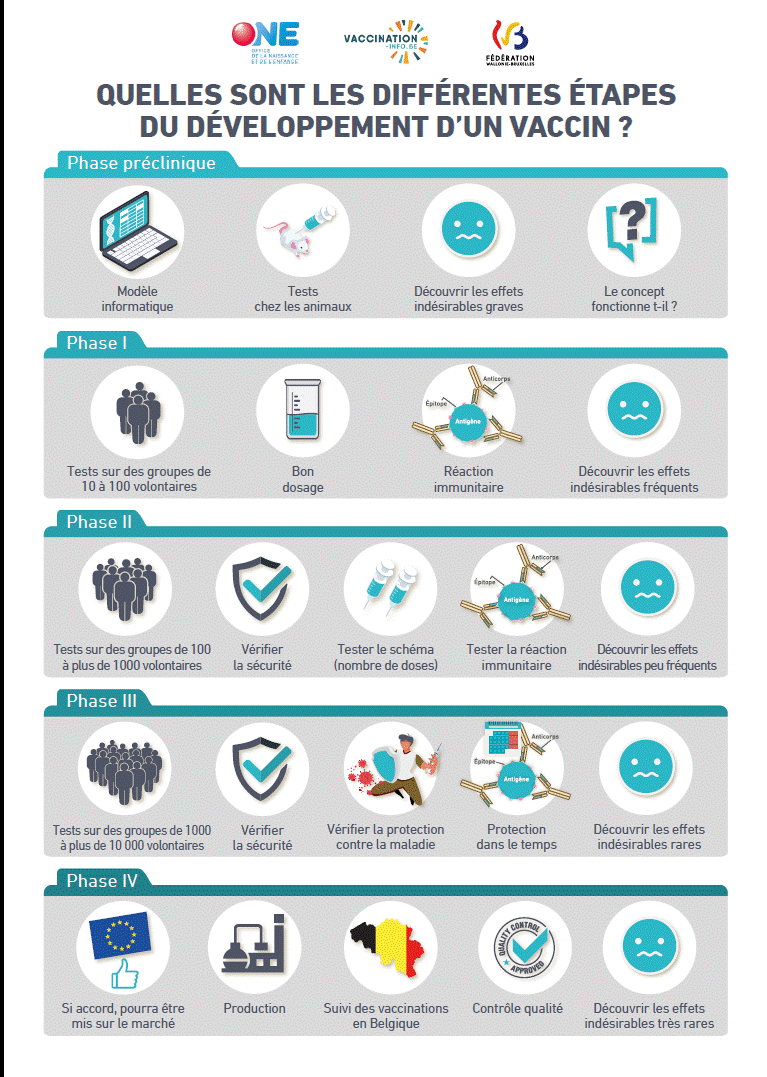
La sécurité des vaccins est un élément essentiel afin de garantir l’adhésion de la population à un Programme de vaccination. Les vaccins utilisés dans les programmes de vaccination sont sûrs et efficaces. Il est toutefois important de rappeler que les vaccins sont des médicaments, et que comme tout médicament, ils peuvent provoquer des effets indésirables. Il y a deux grandes méthodes qui sont utilisées afin d’assurer de la sureté des vaccins : Les essais cliniques ; La vaccinovigilance.
Pour autoriser la mise sur le marché d’un vaccin, les autorités vérifient que la balance bénéfice-risque du vaccin est positive. La tolérance des agences régulatrices (Agence Européenne du Médicament pour l’Union Européenne, Agence Fédérale des Médicaments et des Produits de Santé en Belgique) pour les effets indésirables est très basse car il s’agit d’une intervention préventive. De rares effets sévères et/ou graves peuvent donc être tolérés, si le bénéfice du vaccin dépasse les risques encourus.
La balance bénéfice-risque est évaluée tout au long de la vie du vaccin. Les vaccins font partie des médicaments les plus surveillés.
Les événements de santé survenant après une vaccination sont appelés les MAPIs (manifestation post vaccinale indésirable). Ce sont, par exemple, tous les incidents qui arrivent après une vaccination (symptôme, maladie, résultat anormal dans une sérologie, etc.).
Cela ne veut pas dire relation causale ; cela peut être une coïncidence (relation temporelle). De façon usuelle, on parle d’effets indésirables.